Niewydolność serca ze zmniejszoną frakcją wyrzutową (HFrEF) jest głównym rodzajem niewydolności serca, a badanie China HF Study wykazało, że 42% niewydolności serca w Chinach to HFrEF, chociaż dostępnych jest kilka standardowych klas terapeutycznych leków stosowanych w leczeniu HFrEF, które zmniejszają ryzyko zgonów i hospitalizacji z powodu niewydolności serca. Jednakże u pacjentów występuje wysokie ryzyko nawrotów i zaostrzeń niewydolności serca, śmiertelność utrzymuje się na poziomie około 25%, a rokowanie jest złe. Dlatego nadal istnieje pilne zapotrzebowanie na nowe środki terapeutyczne w leczeniu HFrEF, a w badaniu VICTORIA badano Vericiguat, nowy stymulator rozpuszczalnej cyklazy guanylowej (sGC), aby ocenić, czy Vericiguat może poprawić rokowanie pacjentów z HFrEF. Badanie jest wieloośrodkowym, randomizowanym, prowadzonym w grupach równoległych, kontrolowanym placebo, podwójnie ślepym, opartym na zdarzeniach badaniem III fazy dotyczącym wyników klinicznych. W badaniu, prowadzonym pod patronatem Centrum VIGOR w Kanadzie we współpracy z Instytutem Badań Klinicznych Duke, wzięło udział 616 ośrodków w 42 krajach i regionach, w tym w Europie, Japonii, Chinach i Stanach Zjednoczonych. Nasz oddział kardiologiczny miał zaszczyt wziąć w nim udział. Łącznie 5050 pacjentów z przewlekłą niewydolnością serca w wieku ≥18 lat, II–IV klasa NYHA, EF <45%, z podwyższonym stężeniem peptydu natriuretycznego (NT-proBNP) w ciągu 30 dni przed randomizacją, którzy byli hospitalizowani z powodu niewydolności serca w ciągu 6 miesięcy przed randomizacją lub którym podawano dożylnie leki moczopędne z powodu niewydolności serca w ciągu 3 miesięcy przed randomizacją, wszyscy otrzymali ESC, AHA/ACC i wytyczne krajowe/regionalne zalecają standard opieki. Pacjentów przydzielono losowo w stosunku 1:1 do dwóch grup i podano im lekVericiguat(n=2526) i placebo (n=2524) jako uzupełnienie standardowego leczenia.
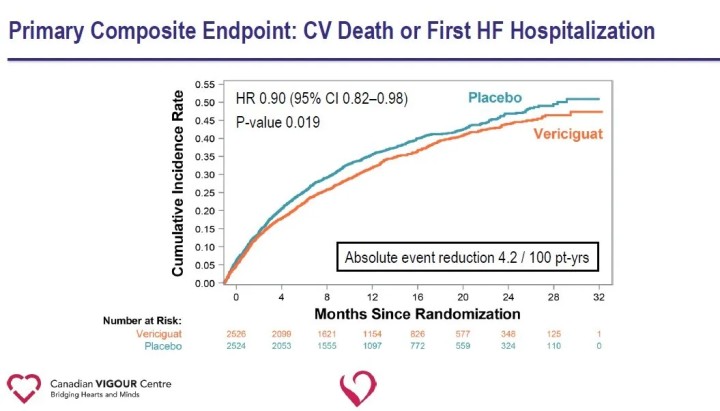
Pierwszorzędowym punktem końcowym badania był złożony punkt końcowy obejmujący zgon z przyczyn sercowo-naczyniowych lub pierwszą hospitalizację z powodu niewydolności serca; drugorzędowe punkty końcowe obejmowały elementy pierwotnego punktu końcowego, pierwszą i kolejne hospitalizacje z powodu niewydolności serca (zdarzenia pierwsze i nawracające), złożony punkt końcowy obejmujący zgon z dowolnej przyczyny lub hospitalizację z powodu niewydolności serca oraz zgon z jakiejkolwiek przyczyny. Po medianie okresu obserwacji wynoszącej 10,8 miesiąca, w grupie otrzymującej Vericiguat w porównaniu z grupą placebo zaobserwowano względne zmniejszenie o 10% głównego punktu końcowego, jakim był zgon z przyczyn sercowo-naczyniowych lub pierwsza hospitalizacja z powodu niewydolności serca.
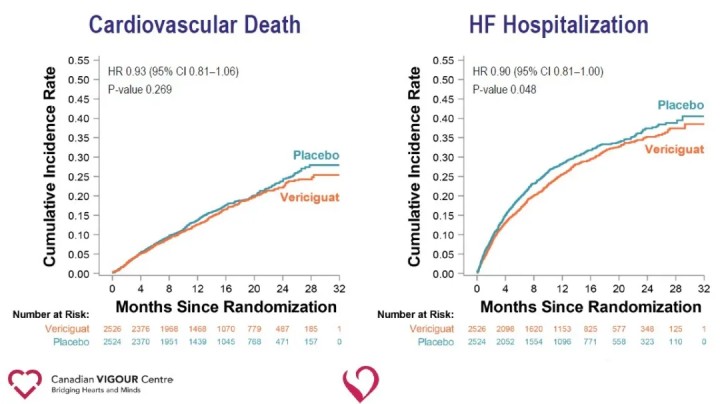
Analiza drugorzędowych punktów końcowych wykazała istotne zmniejszenie częstości hospitalizacji z powodu niewydolności serca (HR 0,90) i istotne zmniejszenie złożonego punktu końcowego obejmującego zgon z jakiejkolwiek przyczyny lub hospitalizację z powodu niewydolności serca (HR 0,90) w grupie otrzymującej Vericiguat w porównaniu z grupą placebo.
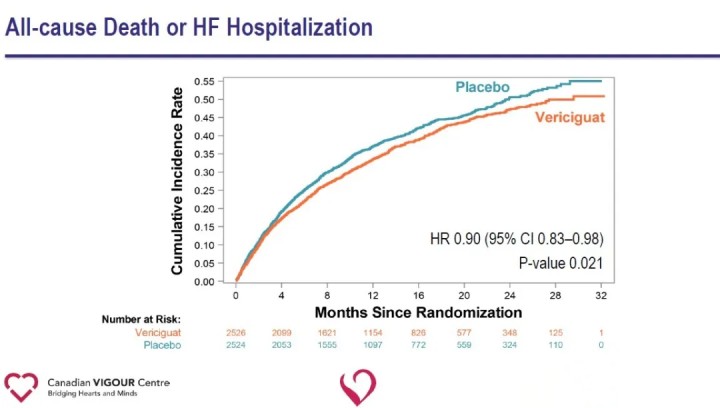
Wyniki badania sugerują, że dodatekVericiguatstandardowe leczenie niewydolności serca znacznie zmniejsza niedawne występowanie pogorszenia się zdarzeń związanych z niewydolnością serca i zmniejsza ryzyko złożonego punktu końcowego, jakim jest zgon z przyczyn sercowo-naczyniowych lub hospitalizacja z powodu niewydolności serca u pacjentów z HFrEF. Zdolność preparatu Vericiguat do zmniejszania ryzyka złożonego punktu końcowego, jakim jest zgon z przyczyn sercowo-naczyniowych lub hospitalizacja z powodu niewydolności serca u pacjentów z niewydolnością serca wysokiego ryzyka, otwiera nową drogę terapeutyczną w przypadku niewydolności serca i otwiera nowe ścieżki przyszłych badań nad chorobami układu krążenia. Vericiguat nie jest obecnie dopuszczony do obrotu. Bezpieczeństwo, skuteczność i opłacalność leku nadal wymagają dalszych testów na rynku.
Czas publikacji: 09 lutego 2022 r
